Après un article introductif sur l’évaluation clinique et un second sur l’application de l’article 61(10) du règlement européen, il est venu le temps de vous présenter 5 Tips (conseils en Français) que j’utilise à chaque rédaction de plan et de rapport d’évaluation clinique.
Ces cinq conseils pourront vous aider dans votre rédaction afin de gagner du temps et de trouver des données de qualité et pertinentes.
Le premier conseil présenté est d’abord de rechercher des dispositifs similaires via des bases de données telles que EUDAMED.
Si vous êtes européennes ou européennes, vous connaissez probablement EUDAMED, la base de données qui permettra (un jour ?) d’avoir accès à des informations sur les dispositifs médicaux disponibles sur le marché. Parmi les modules déjà présents, il y a celui qui permet la « recherche des IUD et les données concernant le dispositif ».
Petite astuce : Pour trouver des produits similaires, utiliser la section « nomenclature » des dispositifs et indiquer le code EMDN de votre produit. Pour filtrer plus de résultats, vous pouvez utiliser les sections : type de dispositif, destination, ou même la classe de risque. Vous tomberez ensuite sur une liste de dispositifs correspondant à votre recherche.
Attention néanmoins, car en fonction du code utilisé, vous pourrez tomber sur des produits très différents du vôtre. Une petite recherche internet sur le dispositif est souvent nécessaire afin de vérifier qu’il est vraiment similaire au vôtre.
Dans la même idée que le premier tips, et même si votre dispositif n’est pas enregistré sur le sol états-unien, des produits similaires peuvent être présents. Deux bases de données sont intéressantes : la GUDID et certains modules du site de la FDA.
La GUDID se présente comme une base de données classique avec des booléens et des mots clés comme le type de produit utilisé, le nom d’un concurrent ou encore le code GMDN ou « Product code ».
Les modules pour le site de la FDA intéressants pour la recherche de concurrents ou de produits similaires sont les suivants :
Petite Astuce : Quand je n’ai pas le code produit FDA, j’utilise la GUDID pour les trouver. Je vais utiliser le nom d’un fabricant concurrent sur le marché, le code GMDN, la classe etc…
Ensuite, j’utilise la base de données du site de la FDA sur la classification du produit et je rentre le code produit recherché, cela m’affichera ici le type de soumission pour le code associé (510K ou PMA).
Et enfin, j’utilise la base de données de soumissions correspondante, je tape le code produit associé, et j’aurais la liste des produits enregistrés pour ce code.
Attention néanmoins, tous les produits enregistrés ne seront pas forcément des produits similaires aux vôtres, ils font juste partie de la même « famille ».
Afin de trouver de potentielles vigilances concernant des produits similaires, vous avez l’option d’aller sur les sites des autorités compétentes comme l’ANSM pour la France et de rechercher dans les informations de sécurité si des produits concurrents apparaissent.
Vous pouvez aussi utiliser le module MAUDE de la FDA (Manufacturer and User Facility Device Expérience). De la même manière que pour le précédent module présenté dans le tips #2, les recherches sont réalisées via des critères comme le code produit. Il est aussi possible d’écrire le nom des produits, du fabricant, les dates de recherche etc…
Vous tomberez ensuite sur une liste où vous pourrez voir des rapports et des descriptions détaillées sur la vigilance.
Comme le mentionne l’article 2 du règlement Européen 2017/745 sur les dispositifs médicaux ainsi que le guide MDCG 2021-6 (Rev.1), une performance est la capacité d’un dispositif à atteindre l’objectif prévu.
La performance clinique, elle, est la capacité d’un dispositif à atteindre l’objectif prévu, conduisant ainsi à un bénéfice clinique.
Chez Cisteo, nous nous intéressons particulièrement à la catégorisation des performances revendiquées du produit pour distinguer explicitement, les performances techniques et les performances cliniques.
Même si le terme de performance technique n’est mentionné ni dans le règlement (EU) 2017/745 ni dans les guides MDCG, on pourrait définir une performance technique par la capacité d’un dispositif à atteindre l’objectif prévu et dont la démonstration se fonde uniquement sur les résultats de méthodes d’essai non cliniques (comme l’évaluation préclinique, les bancs d’essai, …).
En catégorisant ainsi les performances, vous pourrez plus facilement distinguer quelle stratégie clinique doit être appliquée à votre dispositif médical (en se basant sur l’article 61(10) du règlement (EU) 2017/745, sur une équivalence ou sur des données cliniques propres au dispositif médical évalué).
Dans le cadre d’une investigation clinique, cette catégorisation pourrait également vous aider à déterminer qu’elles sont les performances à évaluer.
Le plan et le rapport d’évaluation clinique sont des documents contenant beaucoup d’informations et peuvent facilement faire plus de 100 pages.
Comme dans n’importe quel document faisant partie de la documentation technique : faites des parties sectionnées et n’hésitez pas à faire des tableaux pour synthétiser vos informations. Cela rendra le document plus lisible.
Exemple de présentation d’une synthèse pour la démonstration des performances d’un dispositif médical :
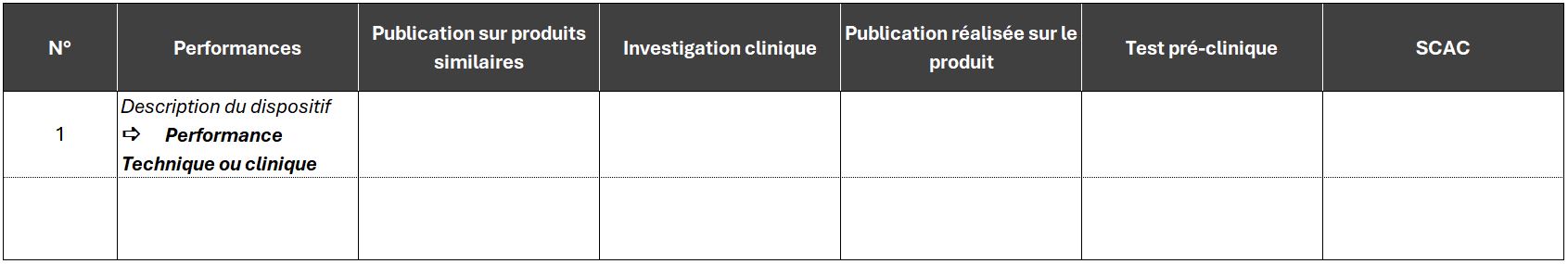
Vous avez besoin d’aide dans la rédaction de votre plan ou rapport d’évaluation clinique ou simplement besoin d’une relecture, nous sommes à votre disposition.
BON A SAVOIR : Notre accompagnement est éligible au dispositif d’aide Diag DM, le dispositif qui finance 50% du montant de la prestation.

